Опис завдання
У цій вправі ти потренуєшся розуміти, як змінюються властивості галогенів зі збільшенням молекулярної маси. Тема важлива для курсів ЗНО з хімії, бо допомагає швидко робити висновки за періодичними закономірностями та не плутатися в типових тестових запитаннях.
На екрані ти бачиш твердження про те, що відбувається у галогенів, коли їхня молекулярна маса зростає. Потрібно уважно прочитати варіанти й обрати правильне спостереження. Такий формат завдання вчить не лише пам’ятати факти, а й мислити логічно: порівнювати елементи однієї групи та робити висновок за трендом.
Ця вправа буде корисною, якщо ти готуєшся до ЗНО або просто хочеш краще розібратися з темою «Флуор, Бром та Йод як представники галогенів». Батькам вона допоможе зрозуміти, що саме тренує дитина: уважність до формулювань, роботу з поняттями «збільшення/зменшення» та вміння відрізняти правильну закономірність від схожих, але хибних тверджень.
- Тренуєш уміння читати умову та обирати правильне твердження з кількох варіантів.
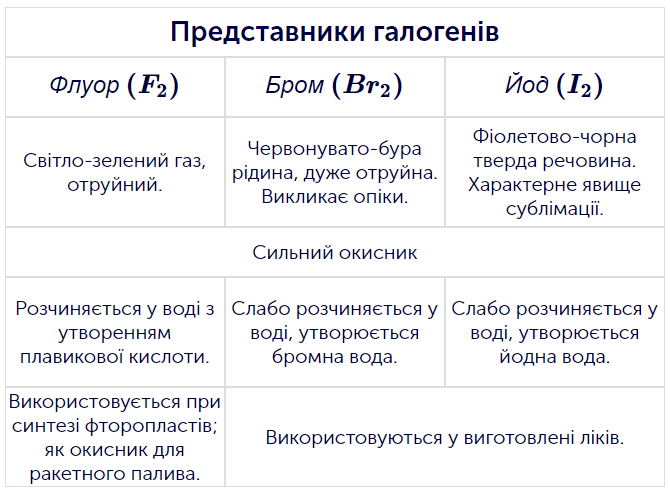
- Закріплюєш знання про властивості галогенів і їхні зміни зі зростанням молекулярної маси.
- Готуєшся до тестового формату ЗНО: швидкість, точність і уважність до деталей.
- Підходить для самостійної роботи вдома та для повторення на уроці.
Учителям ця вправа стане зручною для короткої перевірки розуміння теми або як розминка перед контрольними завданнями. А тобі вона допоможе впевненіше відповідати на питання про закономірності в групі галогенів і не губитися, коли варіанти відповідей дуже схожі між собою.
Пов'язані стандарти
Учасник/учасниця ЗНО повинен/повинна вміти:
- називати найпоширеніші у природі неметалічні елементи; якісний та кількісний склад повітря.
- пояснювати суть явища алотропії; відмінності властивостей алотропних модифікацій Оксигену, Сульфуру, Карбону, Фосфору складом їхніх молекул або будовою; суть явища адсорбції (на прикладі активованого вугілля); антропогенні та природні причини появи в атмосфері оксидів неметалічних елементів, процесів окиснення, колообігу Оксигену;
- наводити приклади алотропних модифікацій Оксигену (кисень та озон), Сульфуру (ромбічна та моноклинна сірка), Карбону (графіт, алмаз та фулерен), Фосфору (білий та червоний фосфор); сполук неметалічних елементів з Гідрогеном (гідроген хлорид, гідроген сульфід, амоніак);
- складати хімічні рівняння, що підтверджують окисні властивості неметалів (кисень, сірка, вуглець, хлор) в реакціях з воднем і металами; відновні властивості водню й вуглецю в реакціях з оксидами металічних елементів; реакцій, які характеризують властивості водних розчинів гідроген хлориду (з основами), гідроген сульфіду (з лугами), амоніаку (з кислотами); реакцій нітратної і концентрованої сульфатної кислот з магнієм, цинком, міддю, реакцій: одержання кисню з гідроген пероксиду та води; кисню з воднем, вуглецем, сіркою, магнієм, залізом, міддю, метаном, гідроген сульфідом;
- порівнювати фізичні та хімічні властивості неметалів, оксидів неметалічних елементів; властивості водних розчинів гідроген хлориду, гідроген сульфіду, амоніаку;
- характеризувати неметали, їхні фізичні властивості та застосування; застосування гідроген хлориду, гідроген сульфіду, амоніаку; фізичні та хімічні властивості нітратної і концентрованої сульфатної кислот (взаємодія з магнієм, цинком, міддю); хімічні властивості кисню; практичну значущість явища адсорбції, адсорбційну здатність активованого вугілля та аналогічних лікарських препаратів;
- оцінювати біологічне значення найважливіших неметалічних (Оксигену, Нітрогену, Карбону, Фосфору, галогенів) елементів; значення кисню в життєдіяльності організмів; озону в атмосфері;
- висловлювати судження щодо застосування озону, екологічних наслідків викидів в атмосферу оксидів Карбону, Нітрогену, Сульфуру; кислотних дощів, парникового ефекту;
- обґрунтовувати значення алотропних перетворень; застосування кисню;
- доводити практичну значущість неметалів та сполук неметалічних елементів.