Опис завдання
Ця вправа допоможе тобі впевнено розібратися з темою «Ароматичність» і зрозуміти, як працюють правила орієнтації замісників у бензольному кільці. Це важлива частина курсу ЗНО з хімії, бо арени мають особливі властивості та реагують не так, як алкани чи алкени. Тут ти потренуєшся правильно формулювати визначення та помічати ключові ознаки ароматичних сполук.
Ароматичність — це сукупність властивостей, характерних для ароматичних вуглеводнів (аренів). У короткому конспекті до завдання зібрані головні «підказки», за якими ти легко впізнаєш ароматичну систему: плоске кільце в молекулі, висока стійкість, делокалізація електронів, а також те, що для аренів типові реакції заміщення, а не приєднання. Окремо зверни увагу на правило Е. Хюккеля, яке пов’язують із проявом ароматичних властивостей у сполуках із плоским кільцем.
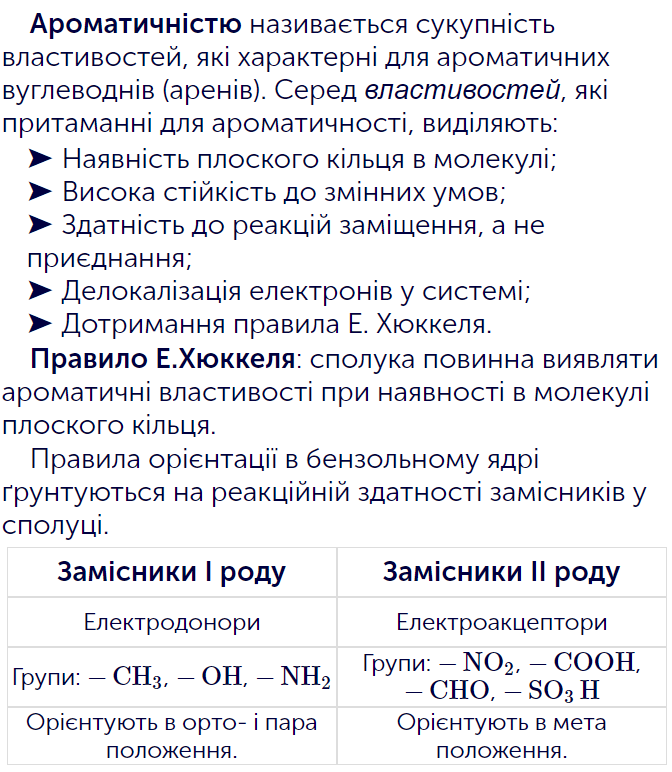
Друга частина матеріалу пояснює орієнтацію замісників у бензольному ядрі. Це потрібно, щоб передбачати, у яке положення (орто, пара або мета) піде новий замісник під час реакції. У вправі ти побачиш дві групи замісників: електродонори та електроакцептори, і навчишся швидко визначати напрям орієнтації.
- Ти закріпиш визначення ароматичності як сукупності властивостей, притаманних аренам.
- Ти запам’ятаєш основні ознаки: плоске кільце, стійкість, делокалізація електронів, реакції заміщення, правило Хюккеля.
- Ти навчишся орієнтувати замісники: електродонори (—CH3, —OH, —NH2) спрямовують у орто- і пара-положення.
- Ти відпрацюєш правило для електроакцепторів (—NO2, —COOH, —CHO, —SO3H), які орієнтують у мета-положення.
Батькам ця вправа зручна тим, що дає чітку опору: короткі формулювання й приклади груп замісників, які легко повторити вдома. Учителям вона стане у пригоді для швидкого повторення перед контролем або як тренажер перед темами про реакції бензену та його похідних. А тобі вона допоможе зібрати тему в логічну схему й не плутатися у визначеннях та напрямках орієнтації.
Пов'язані стандарти
Учасник/учасниця ЗНО повинен/повинна вміти:
- називати загальну формулу ароматичних вуглеводнів;
- розрізняти ненасичені та ароматичні вуглеводні;
- порівнювати зв'язки між атомами Карбону в молекулах бензену та алканів і алкенів, реакційну здатність бензену, алканів, алкенів і алкінів у реакціях заміщення та окиснення; бензену, алкенів і алкінів у реакціях приєднання;
- складати молекулярну та структурну формули бензену; рівняння реакцій, що характеризують хімічні властивості бензену (галогенування, гідрування, горіння), одержання бензену в промисловості (каталітичне дегідрування н-гексану, тримеризація етину).