Опис завдання
У цій вправі ти познайомишся з аренами (ароматичними вуглеводнями) на прикладі найхарактернішого представника — бензену. Саме за бензеном часто пояснюють основні властивості аренів, тому важливо добре розуміти, що це за речовина і як «працює» її будова. Ти пригадаєш молекулярну формулу бензену C6H6 та дізнаєшся про його фізичні властивості: це безбарвна рідина з характерним запахом, легкозаймиста й отруйна.
Далі завдання допоможе тобі розібратися з ізомерією замісників у бензеновому кільці. Коли в кільці є два замісники, важливо, де саме вони розташовані. Положення можна позначати цифрами (1,2; 1,3; 1,4) або словами, які часто трапляються в тестах ЗНО/НМТ: орто-, мета-, пара-. На прикладах ти навчишся швидко визначати, скільки атомів Карбону «розділяє» замісники, і як правильно назвати ізомер.
Вправа на Learning.ua зручна для самоперевірки: ти читаєш коротке пояснення, а потім обираєш або вводиш правильну відповідь. Це тренує уважність до формулювань і допомагає закріпити базові поняття з теми «Властивості аренів» і «Ізомерія замісників у бензені».
- Закріпиш, що бензен — найхарактерніший представник ароматичних вуглеводнів (C6H6).
- Пригадаєш фізичні властивості бензену: безбарвна рідина, характерний запах, легкозаймистість і токсичність.
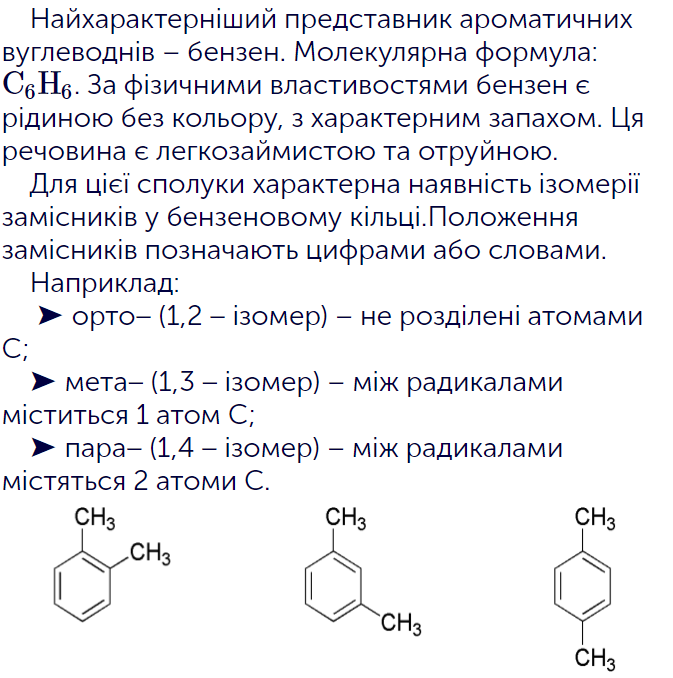
- Навчишся розрізняти орто- (1,2), мета- (1,3) і пара- (1,4) положення замісників у бензеновому кільці.
- Підготуєшся до типових запитань курсів ЗНО з хімії про ароматичні сполуки та їхню ізомерію.
Батькам і вчителям ця вправа стане у пригоді як короткий тренажер перед контрольними та тестами: вона допомагає побачити, чи розуміє учень ключові терміни й чи вміє застосовувати їх на практиці. А тобі вона дасть впевненість у темі, без якої важко рухатися далі в органічній хімії.
Пов'язані стандарти
Учасник/учасниця ЗНО повинен/повинна вміти:
- називати загальну формулу ароматичних вуглеводнів;
- розрізняти ненасичені та ароматичні вуглеводні;
- порівнювати зв'язки між атомами Карбону в молекулах бензену та алканів і алкенів, реакційну здатність бензену, алканів, алкенів і алкінів у реакціях заміщення та окиснення; бензену, алкенів і алкінів у реакціях приєднання;
- складати молекулярну та структурну формули бензену; рівняння реакцій, що характеризують хімічні властивості бензену (галогенування, гідрування, горіння), одержання бензену в промисловості (каталітичне дегідрування н-гексану, тримеризація етину).