Опис завдання
У цій вправі ти потренуєшся швидко знаходити Фосфор у періодичній системі та правильно визначати його місце: період і групу. Завдання має формат тестового запитання з кількома варіантами відповіді, тож воно добре підходить для підготовки до ЗНО з хімії. Ти вчишся не просто «вгадувати», а читати таблицю Менделєєва уважно й упевнено.
Коли ти визначаєш місце елемента, ти повторюєш важливі базові поняття: як нумеруються періоди, що означає група, і як за положенням елемента робити висновки про його властивості. Це корисно не лише для окремого питання про Фосфор, а й для багатьох подібних завдань у тестах, де потрібно швидко орієнтуватися в періодичній системі.
Вправа стане в пригоді учням, які готуються до ЗНО, батькам, що хочуть підтримати навчання вдома, і вчителям для короткої перевірки знань на уроці або під час повторення теми. Працюй у своєму темпі: спочатку знайди Фосфор у таблиці, потім звір період і групу, і лише тоді обирай відповідь.
- Тренуєш уміння знаходити елемент у періодичній системі за назвою.
- Закріплюєш поняття «період» і «група» на реальному прикладі.
- Вчишся працювати з тестовими варіантами та уникати типових помилок.
- Готуєшся до формату ЗНО: швидко, чітко, з опорою на таблицю.
Порада: якщо сумніваєшся, не поспішай. Перевір, у якому рядку таблиці стоїть Фосфор (це і є період), а потім подивись на стовпчик (це група). Так ти будеш відповідати впевнено й зможеш застосувати цей алгоритм для будь-якого елемента.
Пов'язані стандарти
Учасник/учасниця ЗНО повинен/повинна вміти:
- називати найпоширеніші у природі неметалічні елементи; якісний та кількісний склад повітря.
- пояснювати суть явища алотропії; відмінності властивостей алотропних модифікацій Оксигену, Сульфуру, Карбону, Фосфору складом їхніх молекул або будовою; суть явища адсорбції (на прикладі активованого вугілля); антропогенні та природні причини появи в атмосфері оксидів неметалічних елементів, процесів окиснення, колообігу Оксигену;
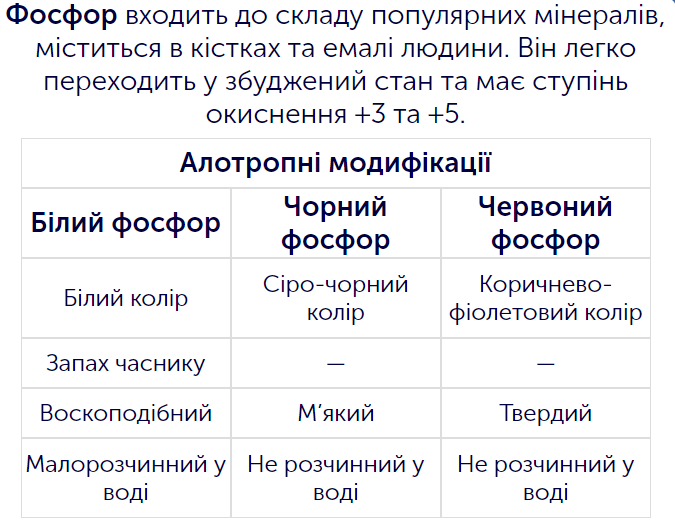
- наводити приклади алотропних модифікацій Оксигену (кисень та озон), Сульфуру (ромбічна та моноклинна сірка), Карбону (графіт, алмаз та фулерен), Фосфору (білий та червоний фосфор); сполук неметалічних елементів з Гідрогеном (гідроген хлорид, гідроген сульфід, амоніак);
- складати хімічні рівняння, що підтверджують окисні властивості неметалів (кисень, сірка, вуглець, хлор) в реакціях з воднем і металами; відновні властивості водню й вуглецю в реакціях з оксидами металічних елементів; реакцій, які характеризують властивості водних розчинів гідроген хлориду (з основами), гідроген сульфіду (з лугами), амоніаку (з кислотами); реакцій нітратної і концентрованої сульфатної кислот з магнієм, цинком, міддю, реакцій: одержання кисню з гідроген пероксиду та води; кисню з воднем, вуглецем, сіркою, магнієм, залізом, міддю, метаном, гідроген сульфідом;
- порівнювати фізичні та хімічні властивості неметалів, оксидів неметалічних елементів; властивості водних розчинів гідроген хлориду, гідроген сульфіду, амоніаку;
- характеризувати неметали, їхні фізичні властивості та застосування; застосування гідроген хлориду, гідроген сульфіду, амоніаку; фізичні та хімічні властивості нітратної і концентрованої сульфатної кислот (взаємодія з магнієм, цинком, міддю); хімічні властивості кисню; практичну значущість явища адсорбції, адсорбційну здатність активованого вугілля та аналогічних лікарських препаратів;
- оцінювати біологічне значення найважливіших неметалічних (Оксигену, Нітрогену, Карбону, Фосфору, галогенів) елементів; значення кисню в життєдіяльності організмів; озону в атмосфері;
- висловлювати судження щодо застосування озону, екологічних наслідків викидів в атмосферу оксидів Карбону, Нітрогену, Сульфуру; кислотних дощів, парникового ефекту;
- обґрунтовувати значення алотропних перетворень; застосування кисню;
- доводити практичну значущість неметалів та сполук неметалічних елементів.