Опис завдання
У цій вправі ти потренуєшся розпізнавати хімічні властивості глюкози та підбирати правильні продукти реакцій. Завдання побудоване у форматі тесту з вибором відповіді: потрібно визначити, що є продуктом часткового окиснення глюкози. Такі питання часто трапляються на ЗНО/НМТ з хімії, бо перевіряють не лише пам’ять, а й розуміння, як поводиться альдегідна група в складі глюкози.
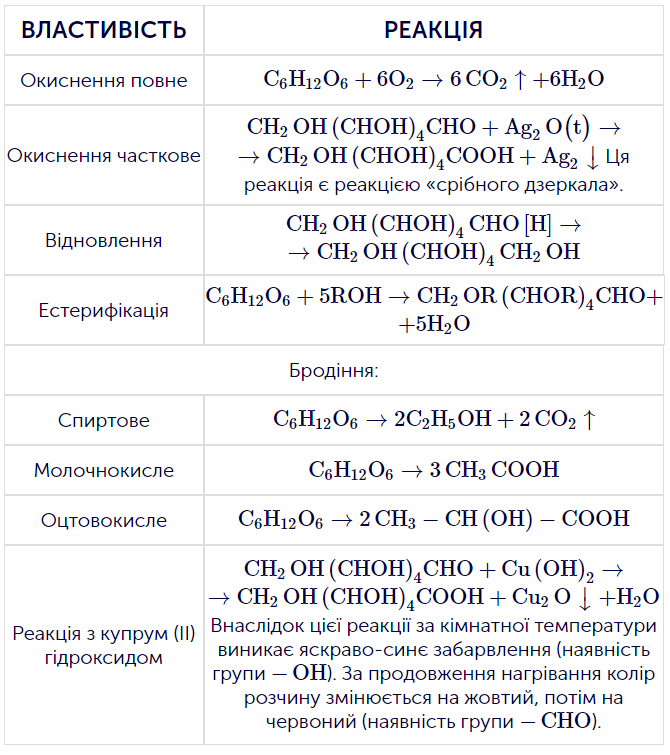
На прикладі реакцій у таблиці ти побачиш різницю між повним і частковим окисненням. Повне окиснення дає вуглекислий газ і воду, а часткове окиснення переводить альдегідну групу –CHO у карбоксильну –COOH, утворюючи глюконову кислоту. Окремо зверни увагу на реакцію «срібного дзеркала» (з Ag2O): це типова якісна реакція на альдегіди, і глюкоза її дає саме завдяки наявності –CHO у відкритій формі.
Вправа також нагадує інші важливі перетворення глюкози: відновлення до багатоатомного спирту (утворення сорбіту), естерифікацію та різні види бродіння. Це допомагає не плутати схожі варіанти відповідей у тестах: наприклад, сорбіт і манніт пов’язані з відновленням, а не з окисненням, тому їх легко відсіяти, якщо ти розумієш тип реакції.
- Закріпиш поняття «повне» та «часткове» окиснення глюкози і їхні продукти.
- Згадаєш реакцію «срібного дзеркала» та ознаки окиснення альдегідної групи.
- Навчишся відрізняти окиснення від відновлення (сorbіт як продукт відновлення).
- Систематизуєш типові рівняння: окиснення, відновлення, естерифікація, бродіння.
- Підготуєшся до тестового формату ЗНО/НМТ: швидко читати умову й обирати правильний варіант.
Батькам і вчителям ця вправа зручна тим, що дає швидку перевірку розуміння теми: дитина не просто вчить формули, а вчиться пояснювати, чому саме глюконова кислота є продуктом часткового окиснення, а CO2 і H2O — результатом повного. Виконуй завдання уважно, звіряйся з рівняннями в таблиці та тренуйся робити висновок за типом реакції — так ти впевненіше почуватимешся на іспиті.
Пов'язані стандарти
Учасник/учасниця ЗНО повинен/повинна вміти:
- розрізняти моно-, ди- та полісахариди;
- пояснювати вплив характеристичних (функціональних) груп на фізичні і хімічні властивості глюкози;
- наводити приклади вуглеводів і їхні тривіальні назви; застосування глюкози, крохмалю (виробництво етанолу), поширення вуглеводів у природі і харчових продуктах;
- складати молекулярну і структурну формулу відкритої форми глюкози, молекулярні формули сахарози, крохмалю і целюлози; рівняння реакцій, що відображають хімічні властивості глюкози (повне і часткове окиснення, відновлення воднем, спиртове та молочнокисле бродіння); сахарози, крохмалю і целюлози (молекулярні рівняння гідролізу), фотосинтезу, утворення сахарози, крохмалю і целюлози у природі;
- порівнювати крохмаль і целюлозу за складом і властивостями;
- застосовувати знання для вибору способу виявлення глюкози (взаємодія з-амоніачним розчином аргентум(І) оксиду, реакції зі свіжоосадженим купрум(ІІ)гідроксидом) і крохмалю (взаємодія з йодом);
- характеризувати хімічні властивості вуглеводів;
- робити висновки щодо властивостей вуглеводів на підставі їхньої будови і про будову вуглеводів на підставі їхніх властивостей та на основі результатів спостережень;
- прогнозувати хімічні властивості вуглеводів на основі знань про властивості характеристичних (функціональних) груп.