Опис завдання
У цій вправі ти тренуєшся визначати тип хімічної реакції за простою схемою. На екрані ти бачиш рівняння у вигляді A + Б = АБ і маєш обрати правильну відповідь серед варіантів: заміщення, розкладу, обміну або сполучення. Це базова навичка для теми «Класифікації хімічних реакцій за складом сполук», яка часто трапляється в завданнях курсів ЗНО з хімії.
Формула A + Б = АБ підказує, що дві речовини з’єднуються в одну. Такі вправи допомагають швидко «зчитувати» тип реакції за загальною схемою, не губитися в позначеннях і не витрачати зайвий час на тесті. Ти вчишся працювати з умовними літерами A і Б, а потім легко переносиш це вміння на реальні приклади з формулами речовин.
Батькам ця вправа зручна тим, що можна швидко перевірити, чи дитина розуміє логіку класифікації: скільки речовин було до реакції і скільки стало після. Учителям вона підходить для короткого повторення на уроці, для домашнього тренування або як міні-діагностика перед контрольними й підготовкою до ЗНО.
- Тренуєш уважність до схеми реакції та вчишся бачити «дві речовини → одна речовина».
- Закріплюєш назви типів реакцій: заміщення, розкладу, обміну, сполучення.
- Розвиваєш навичку швидкого вибору правильної відповіді у тестовому форматі.
- Підходить для самостійної підготовки та повторення перед ЗНО з хімії.
Працюй спокійно: прочитай схему, уяви, що відбувається з кількістю речовин, і вибери варіант відповіді. Коли ти навчишся впевнено визначати тип реакції за такими короткими записами, складніші рівняння стануть значно зрозумілішими.
Пов'язані стандарти
Учасник/учасниця ЗНО повинен/повинна вміти:
- записувати схеми реакцій, хімічні й термохімічні рівняння;
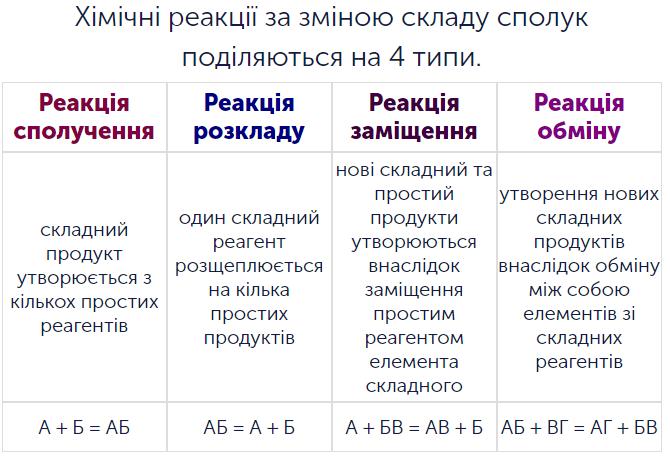
- розрізняти типи реакції за кількістю реагентів і продуктів (реакції сполучення, розкладу, обміну, заміщення), зміною ступеня окиснення елементів (реакції окисно-відновні та без зміни ступеня окиснення), тепловим ефектом (реакції екзотермічні, ендотермічні), напрямом перебігу (реакції оборотні, необоротні); за участю органічних сполук (заміщення, приєднання, відщеплення, ізомеризації);
- аналізувати вплив природи реагентів, їх концентрацій, величини поверхні їх контакту, температури, каталізатора на швидкість хімічної реакції; процеси, що відбуваються при роботі гальванічного елементу;
- визначати в окисно-відновній реакції окисник і відновник, процеси окиснення та відновлення;
- використовувати метод електронного балансу для перетворення схеми окисно-відновної реакції на хімічне рівняння;
- застосовувати закон збереження маси речовин для перетворення схеми реакції на хімічне рівняння, принцип Ле Шательє для визначення напряму зміщення хімічної рівноваги.