Опис завдання
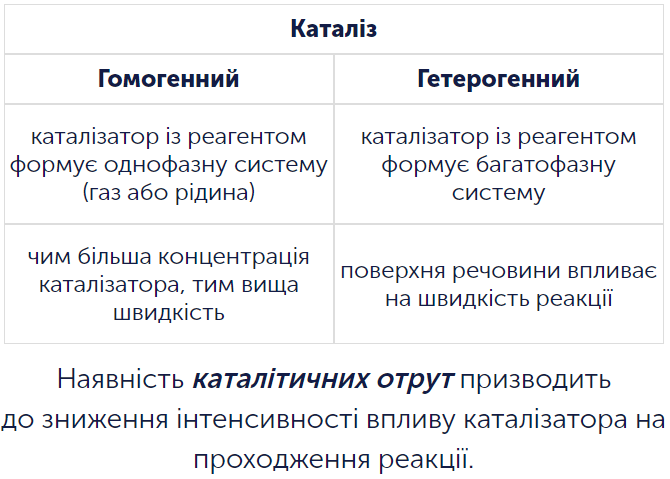
Ця вправа допоможе тобі швидко розібратися з темою «Види каталізу» та закріпити важливе поняття з курсу хімії для підготовки до ЗНО. На екрані ти бачиш завдання: потрібно виділити два види каталізу з поданих варіантів. Такий формат тренує уважність і вміння впізнавати наукові терміни, які часто трапляються в тестах про швидкість хімічної реакції, каталізатори та каталіз.
У завданні подано кілька пар слів, і твоя мета — обрати саме ті, що є реальними видами каталізу. Працюй спокійно: прочитай кожну пару, пригадай визначення та подумай, чи справді так класифікують каталіз у шкільному курсі та в програмі ЗНО. Якщо сумніваєшся, повернись до конспекту: каталіз пов’язаний із тим, у якій фазі перебувають реагенти й каталізатор, і як вони взаємодіють під час реакції.
Для батьків і вчителів ця вправа зручна тим, що дає швидку перевірку базових знань без довгих обчислень. Вона підходить як для повторення перед контролем, так і для короткого щоденного тренування. Учневі важливо не просто «вгадати», а пояснити свій вибір: це формує хімічне мислення та готує до завдань, де потрібно обґрунтовувати відповідь.
- Тренуєш розпізнавання термінів із теми «каталіз».
- Повторюєш класифікації, які використовують у шкільній хімії та на ЗНО.
- Розвиваєш уважність: обираєш правильну пару серед схожих варіантів.
- Зручно для самоперевірки та роботи на уроці або вдома.
Виконуй вправу кілька разів у різні дні: короткі повторення працюють краще за одне довге заняття. А якщо хочеш підсилити результат, після вибору спробуй своїми словами пояснити, що означає кожен обраний вид каталізу та як він пов’язаний зі швидкістю хімічної реакції.
Пов'язані стандарти
Учасник/учасниця ЗНО повинен/повинна вміти:
- записувати схеми реакцій, хімічні й термохімічні рівняння;
- розрізняти типи реакції за кількістю реагентів і продуктів (реакції сполучення, розкладу, обміну, заміщення), зміною ступеня окиснення елементів (реакції окисно-відновні та без зміни ступеня окиснення), тепловим ефектом (реакції екзотермічні, ендотермічні), напрямом перебігу (реакції оборотні, необоротні); за участю органічних сполук (заміщення, приєднання, відщеплення, ізомеризації);
- аналізувати вплив природи реагентів, їх концентрацій, величини поверхні їх контакту, температури, каталізатора на швидкість хімічної реакції; процеси, що відбуваються при роботі гальванічного елементу;
- визначати в окисно-відновній реакції окисник і відновник, процеси окиснення та відновлення;
- використовувати метод електронного балансу для перетворення схеми окисно-відновної реакції на хімічне рівняння;
- застосовувати закон збереження маси речовин для перетворення схеми реакції на хімічне рівняння, принцип Ле Шательє для визначення напряму зміщення хімічної рівноваги.