Опис завдання
У цій вправі ти потренуєшся швидко впізнавати кислоти за хімічною формулою. На екрані подано кілька речовин, і твоє завдання просте: серед формул KH2PO4, HClO4, CaO, CuOHNO3 вибрати саме кислоту. Такі міні-завдання добре розвивають уважність і допомагають закріпити тему про склад і номенклатуру кислот, що важливо для підготовки до ЗНО з хімії.
Щоб правильно відповісти, згадай головну ознаку: кислоти зазвичай починаються з атома Гідрогену (H) і в розчині можуть віддавати йони H+. Але будь уважним: не кожна формула з H обов’язково є кислотою, а деякі речовини з H можуть бути солями або основними солями. Тому в цій вправі ти вчишся не вгадувати, а перевіряти формулу логічно.
Для батьків і вчителів ця вправа зручна тим, що її можна виконувати за 1–2 хвилини, а потім коротко обговорити відповідь: чому обраний варіант є кислотою, а інші — ні. Це формує вміння класифікувати речовини та пояснювати свій вибір, що часто потрібно на тестах і під час розв’язування задач.
- Тренуєш розпізнавання кислот за формулою серед різних класів неорганічних сполук.
- Повторюєш ознаки кислот і відрізняєш їх від оксидів, солей та сполук з гідроксогрупою.
- Розвиваєш навичку швидкого аналізу формул — корисно для тестових завдань ЗНО.
- Вчишся аргументувати відповідь, а не просто обирати навмання.
Виконуй вправу кілька разів, щоб діяти впевнено: спочатку знайди, з чого починається формула, потім оціни, чи може речовина бути кислотою за складом, і лише тоді обирай відповідь. Якщо помилився — це нормально: повернись до правил і спробуй ще раз. Так знання про кислоти, їхній склад і назви запам’ятовуються надовго.
Пов'язані стандарти
Учасник/учасниця ЗНО повинен/повинна вміти:
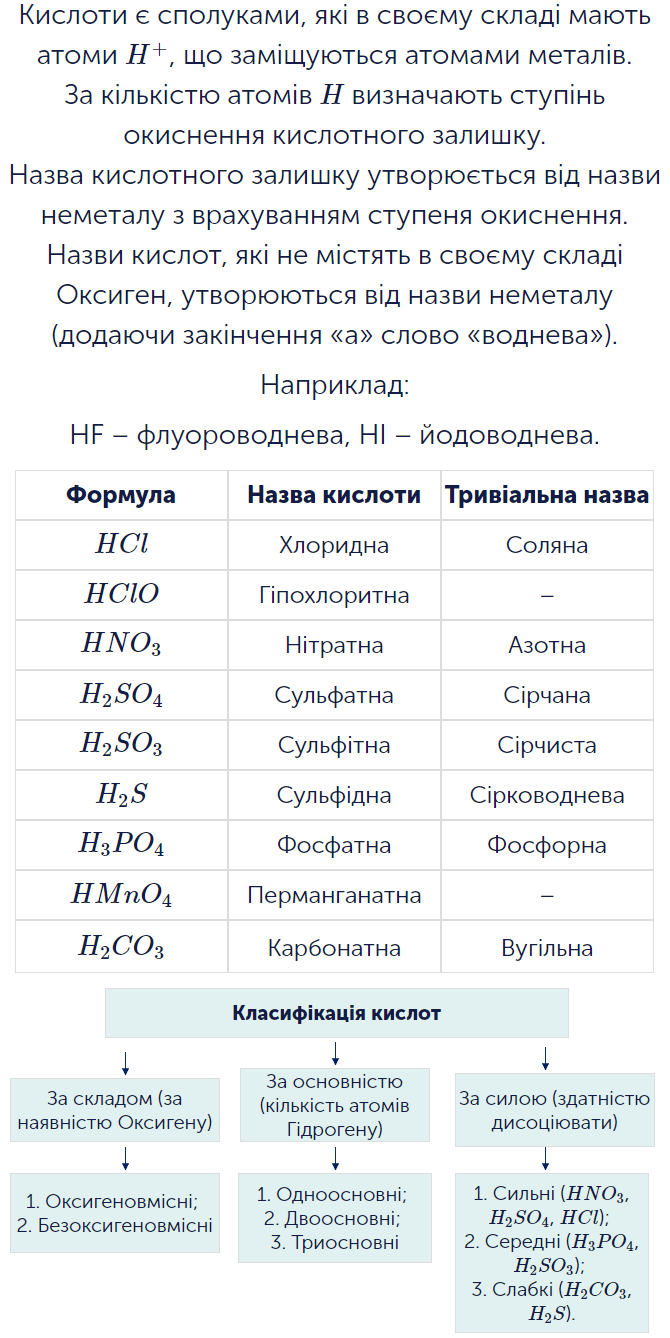
- називати кислоти за сучасною науковою українською номенклатурою за їхніми хімічними формулами;
- розрізняти кислоти за складом (оксигеновмісні, безоксигенові), основністю (одно-, дво-, триосновні), здатністю до електролітичної дисоціації (сильні, слабкі);
- складати хімічні формули кислот; рівняння реакцій, які характеризують хімічні властивості кислот (взаємодія з металами, основними, та амфотерними, оксидами, основами та амфотерними гідроксидами, солями) та способи їх одержання (взаємодія кислотних оксидів із водою, деяких неметалів із воднем, солей із кислотами);
- характеризувати фізичні властивості кислот;
- визначати формули кислот серед формул сполук інших вивчених класів, валентність кислотного залишку за формулою кислоти;
- прогнозувати можливість перебігу хімічних реакцій кислот з металами, використовуючи ряд активності металів.