Опис завдання
У цій вправі ти потренуєшся визначати тип кристалічних ґраток на прикладі води. На екрані є запитання: «Вкажи тип кристалічних ґраток у молекулі води» та варіанти відповіді: атомний, молекулярний, металічний, йонний. Це коротке завдання з вибором відповіді допомагає швидко перевірити, чи розумієш ти, як будова речовини пов’язана з її властивостями.
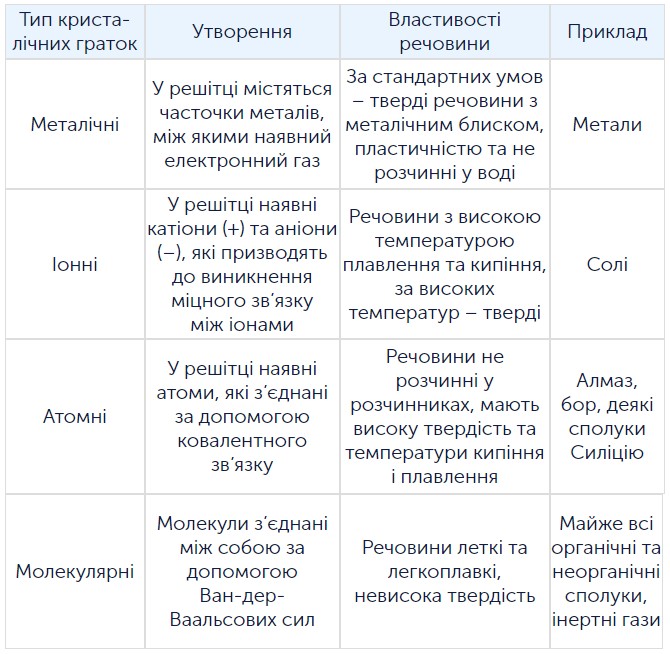
Тема «Кристалічні ґратки та властивості речовини» важлива для курсів ЗНО з хімії, бо часто трапляється в тестах. Тобі потрібно не просто запам’ятати назви, а навчитися впізнавати тип ґраток за тим, з яких частинок складається речовина та які зв’язки між ними переважають. У води в твердому стані частинки розміщуються впорядковано, і від цього залежать такі властивості, як температура плавлення, крихкість, електропровідність.
Вправа зручна для самоперевірки: ти обираєш один варіант і одразу бачиш, чи правильно міркуєш. Батькам це допоможе зрозуміти, що саме дитина повторює перед іспитом, а вчителям — швидко дати учням коротке тренування на уроці або як домашнє завдання.
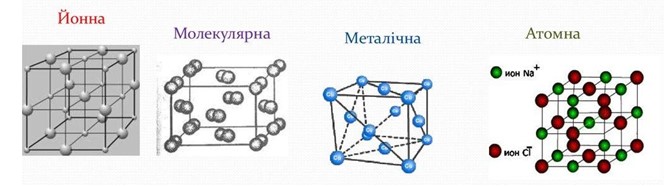
- Закріплюєш поняття про типи кристалічних ґраток: атомні, молекулярні, металічні, йонні.
- Вчишся уважно читати формулювання та обирати правильну відповідь у форматі тесту ЗНО.
- Тренуєш логіку: зіставляєш будову речовини з її властивостями.
- Підходить для швидкого повторення, розминки на початку уроку або підсумку теми.
Виконуй завдання спокійно: прочитай запитання, згадай, які частинки утворюють ґратку, і лише потім обирай відповідь. Так ти поступово сформуєш навичку, яка дуже допомагає на ЗНО: не вгадувати, а впевнено визначати правильний варіант.
Пов'язані стандарти
Учасник/учасниця ЗНО повинен/повинна вміти:
- наводити приклади речовин із різними видами хімічного зв'язку; аморфних і кристалічних речовин;
- пояснювати відмінності в механізмах утворення ковалентних зв'язків у молекулі амоніаку та йоні амонію; між аморфними і кристалічними речовинами;
- розрізняти обмінний та донорно-акцепторний (катіон амонію) механізми утворення ковалентного зв'язку;
- складати електронні формули молекул, хімічні формули сполук за зарядами йонів;
- установлювати види хімічного зв'язку в речовинах за їхніми формулами;
- визначати прості, подвійні, потрійні, полярні та неполярні ковалентні зв'язки між атомами;
- прогнозувати вид хімічного зв'язку в сполуці, можливість утворення водневого зв'язку між молекулами, фізичні властивості речовин на основі їхньої будови та будову речовин на основі їхніх фізичних властивостей (типу кристалічних ґраток);
- оцінювати на основі будови молекул води і спиртів можливість утворення водневого зв'язку між молекулами води, органічних речовин, води і органічних речовин.